Discussions concernant le processus diagnostic
La découverte de la splénomégalie à l’examen physique et à l’IRM abdominale a orienté les étapes diagnostiques ultérieures. Compte tenu de la corrélation avec le tableau clinique et les examens de laboratoire, en particulier la cytopénie bilinéaire (anémie et leucopénie avec neutropénie), il a été émis l’hypothèse que l’hyperplasie splénique pourrait être liée à des infections systémiques. Les formes infiltratives oncologiques-hématologiques et les pathologies avec altération de la régulation immunitaire telles que le lupus érythémateux systémique et le syndrome de Felty ont été exclues en raison de l’absence de critères diagnostiques.
Le degré de cytopénie ne corrélait pas avec la splénomégalie, qui, bien que présente, était légère. Cela a conduit à envisager une condition directement responsable de la cytopénie, comme on l'observe dans certaines infections telles que les zoonoses.
Une consultation en hématologie a été demandée, recommandant une ponction de moelle osseuse et une culture pour clarifier l’étiologie de la fièvre. Le 22 mars 2024, le patient a subi une ponction de moelle osseuse pour la cytomorphologie, la cytométrie en flux, la culture de la moelle et la recherche d’agents zoonotiques. L'examen a révélé la présence répandue de Leishmania à l’intérieur et à l'extérieur des cellules ; un résultat compatible avec la Leishmaniose.
Le diagnostic de leishmaniose viscérale a donc été posé. Chez ce patient, la manifestation viscérale, caractérisée par une splénomégalie et une cytopénie due à l’atteinte médullaire, a été exacerbée par l’immunosuppression causée par le traitement chronique aux stéroïdes pour son anémie hémolytique auto-immune.
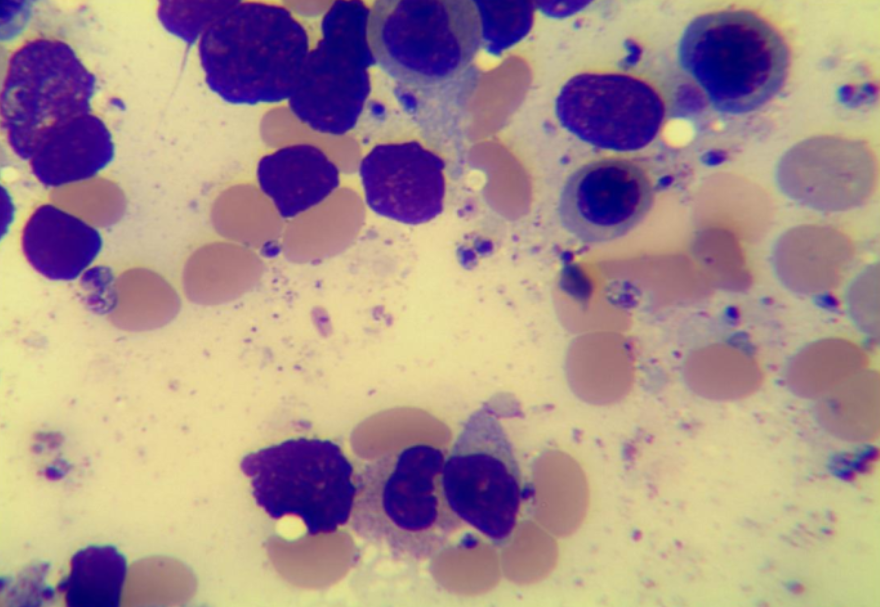
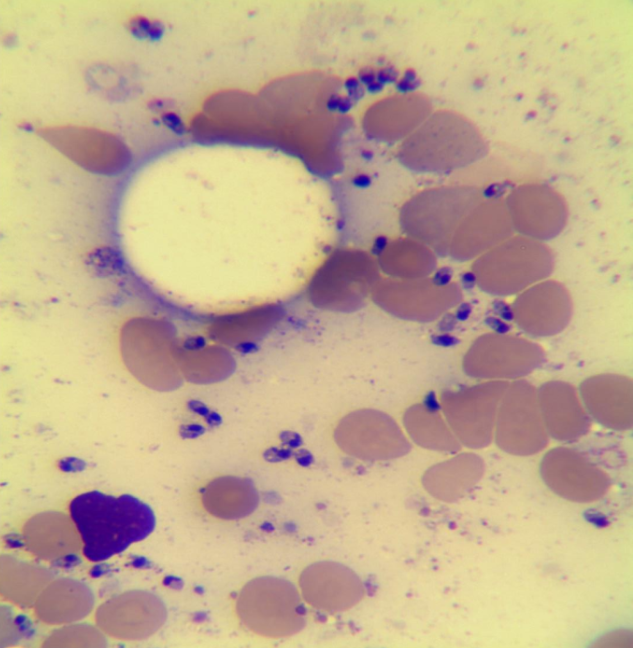
Examen de la moelle osseuse - Le schéma morphologique global décrit une moelle hématopoïétique hyperplasique avec des signes d’infection parasitaire compatibles avec Leishmania.
Le patient a été traité par AmBisome (Amphotéricine B liposomale) 250 mg/jour pendant 5 jours. Après le traitement, le patient a montré une amélioration progressive de son état clinique général, une disparition de la fièvre et une amélioration des tests de laboratoire, jusqu’à la normalisation des valeurs de la NFS et des indices de cytolyse hépatique. Le patient est sorti de l'hôpital le 29 mars.
La leishmaniose viscérale
La leishmaniose est une maladie parasitaire causée par une infection par des parasites Leishmania, qui se propage par la piqûre de mouches des sables infectés. L’infection est endémique dans 90 pays, tropicaux et subtropicaux ainsi qu’en Europe du Sud, notamment dans le bassin méditerranéen. La transmission se fait généralement par la piqûre de femelles hématophages de certaines espèces de phlébotomes des genres Phlebotomus (Europe, Asie et Afrique) et Lutzomyia (Amériques).
Les chiens constituent le principal réservoir du parasite. D’autres espèces domestiques (par exemple, chat, cheval et bétail) et sauvages (par exemple, renard et rat) peuvent rarement manifester la maladie mais ne semblent pas servir de réservoirs.
Les manifestations cliniques sont diverses : la forme cutanée, la forme muco-cutanée et la forme viscérale. La forme cutanée et muco-cutanée peuvent être considérées comme des manifestations à évolution bénigne, tandis que la forme viscérale présente des manifestations systémiques plus graves.
La forme viscérale se manifeste le plus souvent de manière asymptomatique ; les facteurs de risque d’infection incluent les maladies hématologiques malignes, l’âge infantile, la transplantation, l’infection par le VIH et les traitements immunosuppresseurs.
Le risque de manifestation de la leishmaniose viscérale après infection dépend de plusieurs facteurs, le plus significatif étant l’immunocompétence. C’est pourquoi la leishmaniose viscérale est associée aux conditions immunosuppressives.
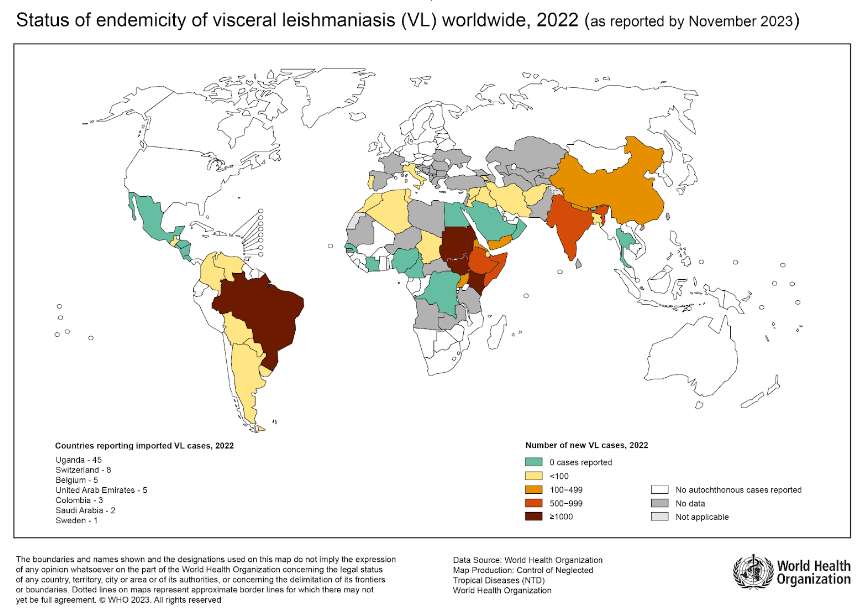
Une fois infectée, Leishmania se réplique dans le système réticulo-endothélial ; une charge parasitaire très élevée s’accumule dans la rate, le foie et la moelle osseuse.
Une anémie sévère peut alors survenir en raison de la suppression de la moelle osseuse, de l’hémolyse et de la séquestration splénique, associée à une neutropénie et une thrombocytopénie.
L’infection a une période d’incubation de 2 à 6 mois, et le début de la maladie est presque jamais aigu, mais se présente plutôt de manière insidieuse et subaiguë, avec une symptomatologie non spécifique caractérisée par de la fièvre, un malaise général, une asthénie avec une évolution progressive, une perte de poids, une anémie ; une splénomégalie et des sueurs nocturnes sont parfois présentes.
À mesure que la maladie progresse, une pancytopénie est observée avec des complications hémorragiques, des infections bactériennes secondaires, ainsi qu’une cachexie et une dysfonction organique.
Sans traitement, le taux de mortalité lorsque la maladie devient manifeste est supérieur à 90%.
La thérapie de soutien vise à maintenir l’état nutritionnel, à gérer l’anémie, les complications hémorragiques et les infections secondaires. L’amphotéricine B liposomale est le médicament le plus efficace avec un profil de sécurité supérieur, sans les effets toxiques de la forme standard (risque élevé de toxicité rénale).
La leishmaniose viscérale est une condition rare mais possible, notamment dans les régions endémiques telles que le sud de l’Italie. La leishmaniose est classée comme une maladie tropicale négligée par l’Organisation mondiale de la santé. Cependant, environ 700 000 à 1 million de nouveaux cas surviennent chaque année. Ces chiffres pourraient augmenter en raison du changement climatique. L'augmentation des températures dans les régions tempérées pourrait à l’avenir attirer les phlébotomes, qui trouveraient alors de nouveaux habitats.
Informations complémentaires : Mises à jour sur la leishmaniose émises par l’OMS